胸水の原因は?
問題110
82歳、男性が胸水の精査目的で受診。
既往歴:18年前に急性心筋梗塞を発症しステント留置術を施行され、以後、当院循環器内科で経過観察中。2型糖尿病に対して近医通院中。結核の既往はない。当院の定期薬はアスピリン(バイアスピリン®)100 mg 1錠/日、プラバスタチン(メバロチン®)10 mg 1錠/日、シロスタゾール(プレタールOD®)100 mg 2錠/日
飲酒歴:なし。喫煙歴:60歳まで1箱/日、以後禁煙。家族歴:特記事項なし。
現病歴:冠動脈ステント留置施行後、当院循環器内科でそれに関する経過観察中であった。2か月前の胸部CTで左少量胸水を指摘されたが、今回再検したところ軽度増加していることが判明したため呼吸器内科に紹介となった。たまに咳嗽がある。
現症:身長 152.0 cm、体重 52.0 kg。血圧120/77 mmHg、脈拍65/分、体温36.8℃、SpO2 94%。皮膚、可視粘膜に貧血、黄疸なし。肺野:清。心音:整、病的雑音聴取せず。腹部:平坦、軟、腸蠕動正常。肝脾触知せず。下肢に浮腫なし。
検査所見:血液所見:白血球5700/μL(好中球54.0%、リンパ球33.6%、単球8.8%、好酸球3.2%、好塩基球0.4%)、赤血球394万/μL、Hb 11.4 g/dL、Hct 34.3%、血小板19.5万/μL。血液生化学検査:CRP 0.09 mg/dL、LDH 218 U/L、AST 43 U/L、ALT 46 U/L、ALP 432 U/L(基準110~360)、γ-GTP 524 U/L、T-Bil 0.4 mg/dL、T-P 7.5 g/dL、Alb 3.9 g/dL、AMY 73 U/L、CPK 121 U/L、BUN 27 mg/dL、Cr 1.34 mg/dL、eGFR 39.7 mL/min、CYFRA21-1 3.1 ng/mL(基準0~3.5)、 CEA 1.3 ng/mL(基準0~5.0)、CA19-9 11.7 U/mL(基準0~37.0)、ProGRP 58.2 pg/mL(基準0~80.9)、IL-2-R 1532 U/mL(基準135~483)
胸水検査所見
性状:淡々血性微濁、比重1.014、pH 8.5、蛋白 3.2 g/dL、糖 163 mg/dL、リバルタ(-)、LDH 175 U/L、ADA 17.3 U/L、CEA 0.5 ng/mL、RF(-)、細胞数 350/μL
細胞分類:リンパ球81%、好中球7%、マクロファージ1%、その他10%
細菌培養は一般細菌、抗酸菌とも培養されず。
胸水cell blockでのHE染色(図1-a)、TIF-1染色(図1-b)、カルレチニン染色(図1-c)を示す。
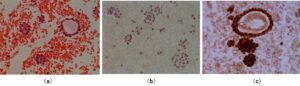
図1
画像所見
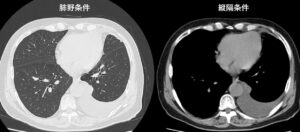
図2:胸腹部CT ここに示す所見以外に明らかな異常を認めなかった。
FDG-PETでは異常な集積を認めなかった。
問題
最も考えられる疾患はどれか。1つ選べ。
(a)肺腺癌
(b)転移性肺癌
(c)悪性胸膜中皮腫
(d)肺小細胞癌
(e)神経内分泌癌
(類題 2016年総合内科専門医試験問題)
解説
画像的に見て左の片側胸水であることや肺門部の血管怒張もないことから心不全の胸水ではなさそうである。血清アルブミンも3.9 g/dLあり、肝腎機能不全もなさそうなデータであり、下腿浮腫なくCPKなども正常であることから、甲状腺機能低下もなさそうである。これらの状況からは漏出性胸水ではなさそうであり、さらに精査を進めるためにはやはり胸水穿刺で胸水に関する分析をしていく必要がある。
まず胸水を穿刺して検査に提出したらLightの基準に照らして胸水が滲出性か漏出性かを鑑別する。Lightの基準は、以下の3項目のうち少なくとも1項目を満たせば滲出性、いずれも満たさなければ漏出性と判断する。
◾胸水TP/血清TP>0.5
◾胸水LDH/血清LDH>0.6
◾胸水LDHが血清LDH上限値の2/3以上
今回の症例では胸水TP/血清TPは3.2/7.5=0.42で満たさず、胸水LDH/胸水LDHは175/218=0.80で満たし、胸水LDHである175 U/Lは血清LDHの上限値である245 U/Lの2/3以上あるので満たす、ということで3項目のうち2項目を満たし、やはり滲出性である。ADAの上昇はなく結核性胸膜炎は否定的である。胸水中には、リンパ球、好中球、マクロファージのいずれにも分類できない細胞が10%検出されており、これが何であるかを追求したい。そこで胸水細胞診を提出したところ最初の報告ではadenocarcinomaが疑われると診断されたのであるが、今回の問題では、セルブロックの組織像を提示している。セルブロックは細胞診塗沫標本作製後に残存する細胞沈渣を種々の基材とともに凝固・固化、あるいは遠心分離することによって集塊状とし、ホルマリン固定、パラフィン包埋を行い、組織検体のようなパラフィンブロックを作製したものである。胸水のような体腔液や、生検不可能な組織からの穿刺吸引細胞診検体が対象となる。提示された組織像をみるとN/C比の高い異型性のある上皮様細胞の集塊が多数みられ、一部は腺管様構造をとっており、核分裂像もわずかに認められた。
胸水から腺癌が疑われる細胞が検出されれば、通常は胸膜腔ではなく、どこか別の臓器に原発巣があってその胸膜転移であろうと考える。ところが、通常のCT検査でもPET-CTでも原発巣と疑えるところが見当たらなかった。その場合、原発巣の腫瘍が微小で胸膜腔という転移先で活発に増殖した結果としてこのような所見となる場合、さらには胸膜腔自体に原発する唯一の癌腫として腺管様構造を呈する胸膜中皮腫の場合、のいずれかを考えなければならない。そこでそのような鑑別疾患を考えながら、あとはセルブロックから複数の組織切片を作成し、各種マーカーを免疫染色することによって、原発巣を推測していくことになる。
まずTIF-1は、肺原発の腫瘍であることの確認に用いられる。肺癌の中で、腺癌(80%程度)、小細胞癌(90%程度)、カルチノイド(50%以上)、大細胞性神経内分泌細胞癌(約50%)、大細胞癌では低率(10%以下)である。肺扁平上皮癌では通常陰性(10%以下には陽性)となり、中皮腫では陰性であるため、肺腺癌との鑑別に特に有用である。さらにカルレチニンは悪性中皮腫に強い陽性反応を示す。腺癌での陽性率は低率(10%)であり、現在、中皮腫の最も有用性が高いマーカーと言われている。今回の症例ではTIF-1陰性、カルレチニン強陽性、そのほかcytokeratin-7陽性、などがみられ、最終的には腺癌ではなく、悪性胸膜中皮腫と診断された。まだCT、PET-CTで検出できないような微小な段階での腫瘍性病変から胸水の貯留する胸膜腔へと細胞が脱落していった結果、胸水中に多数の中皮腫細胞が検出されたのではないかと考えられた。
その後、組織学的に確定診断をつけるため、他院の胸部外科に紹介のうえ、胸腔鏡下胸膜生検を施行いただいた。その結果、上皮成分と間葉系成分を含む二相性の像を呈する悪性中皮腫と最終診断された。
胸膜中皮腫は、胸膜に発生する悪性腫瘍であり、胸膜に原発する唯一の癌腫である。多くは建材(建築物に使用)、摩擦材(ブレーキに使用)、パイプ材(下水道管に使用)、断熱材(ボイラーに使用)などに広く使用されているアスベスト(石綿)の吸引により、20~40年を経て発症すると考えられている。石綿は、現在では中皮腫や肺癌の原因と考えられているため使用が禁止されているが、1970~90年代に建てられた建築物には広く使用されており、今後これらの老朽化による解体作業時の暴露の機会などが増えるために増加が予想されている。アスベスト労働者が胸膜中皮腫を発症する頻度は10%とされている。喫煙とは関係しない。しかし今回の症例では職業上、はっきりとしたアスベスト暴露歴はなかった。この20年で4倍に増加、年間死亡者数は1500人で高齢の男性に多い。種々の呼吸器症状や胸部圧迫感、胸痛などの他、無症状で偶然健診でひっかかる場合もある。一般に中皮腫と診断される症例の90%は胸膜型中皮腫であるが、まれに心膜型、腹膜型もある。診断としては、まず胸部レントゲン検査やCT検査で胸膜の肥厚や胸水貯留で本症を疑い、胸膜組織や腫瘍組織を採取して病理学的に確定診断をつける。胸膜生検の方法として、経皮的針生検が行われるが、十分な組織採取を目的に胸腔鏡下生検、あるいは開胸生検などが行われる場合もある。胸水の細胞診でも診断がつく場合もあり、今回の症例でもほぼ細胞診と採取細胞を集めたセルブロックでの病理診断でほぼ診断がついているが、他の疾患との鑑別が病理学的に困難な場合が多い。組織型によって、乳頭状の腫瘍細胞の発育を呈する上皮型、紡錘形の腫瘍細胞の発育がみられる肉腫型、上皮型(上皮型成分)と肉腫型(間葉系成分)の混在を呈する二相型に分けられており、今回の症例は二相型であったが、上皮型が最も多い。胸水中ヒアルロン酸値の上昇は参考にはなるが、さまざまな疾患で上昇がみられ確定診断にはならない。治療は、シスプラチン(シスプラチン®、ランダ®)+ペメトレキセド(アリムタ®)などの抗癌剤や放射線療法、特に片側肺で合併症がない場合には胸膜肺全摘除術、などが単独あるいは組み合わせて行われている。化学療法後の増悪例には免疫療法としてニボルマブ(オプジーボ®)も保険収載されている。高齢者では対症療法で経過をみる場合もある。予後は9~12か月とされているが症例によってさまざまである。
原因として石綿吸引の既往が職業歴から疑われる場合は、労災保険、石綿健康被害救済制度の適応となりうる。
解答
(c)

