悪性リンパ腫治療前に
問題99
65歳の男性がB細胞悪性リンパ腫の診断で抗CD抗体製剤リツキシマブも併用したCHOP療法を予定されている。これまで感染症関連項目で判明している検査は、HBs抗原、HCV抗体、RPR定性法のみ行われており、すべて陰性であった。
追加する必要のない検査はどれか。2つ選べ。
(a)HBs抗体
(b)HBc抗体
(c)HBe抗体
(d)HBe抗原
(e)HA抗体
解説(オリジナルは『Dr. Tomの内科症例検討道場』第4版の症例42)
まずB型肝炎ウイルスの自然経過を示す(図1)。無症候性HBキャリアの時期は、HBe抗原陽性、HBe抗体陰性で、ウイルス量も多いが、ウイルスが存在してもそれに対して宿主の免疫が反応せずウイルスと宿主の肝細胞とが共存共栄し(免疫寛容)、肝炎はおこらない。無症候性キャリアは自然経過でその多くは10歳代後半から20歳代でこの免疫寛容期から免疫排除期(肝炎によりウイルスを排除していく時期)へと移行し、ここで肝炎を発症する。この肝炎により85~90%はHBe抗原陰性、HBe抗体陽性へとHBe抗原のセロコンバージョンが起こりウイルス量も低下、肝炎は鎮静化し、非活動性キャリアとなる。さらにこの非活動性キャリアを経過した後、一部の症例ではHBs抗原が陰性化し、回復期に入る。一方、無症候性キャリアのうち10~15%は、肝炎が生じるにもかかわらずウイルス量が十分低下せず、その後も肝炎が持続するため、これが慢性肝炎、さらには肝硬変へと進展し、肝細胞癌発症の高リスク群となる。
ここで非活動性キャリアでは宿主免疫が優位となりHBVの増殖を持続的に抑えてくれるため肝炎が鎮静化してくれて、ようやく一安心、ということになるのだが、自然経過や宿主の免疫が抑制された状態になるとB型肝炎が再活性化する。また自然経過の中でHBs抗原が陰性化して回復期に入っても、HBVはHBV cccDNAと呼ばれるいわばウイルスのかけらのようなものとして残存し、通常の免疫監視下では目立ったHBVの増殖はおこらないが、免疫抑制下ではcccDNAを起点にHBVの増殖が起こり、肝炎が再燃する。このような肝炎をde novo B型肝炎と呼ぶ。この肝炎再燃は、回復期でHBs抗原陰性の症例だけでなくさらにHBs抗体陽性になっていても起こりうるため、基本的にウイルスがどのような状態であれHBVに感染したことのある患者は全ておこしうること、かつこのde novo B型肝炎は通常のB型肝炎に比べて劇症化する頻度が高率(27% vs 7%)で、死亡率も高いこと(劇症肝炎となった場合の死亡率100% vs 44%)に注意したい。
さて今回の症例であるが、B細胞性悪性リンパ腫に対して、リツキシマブを併用したCHOP療法が予定されているということであるため、リツキシマブとプレドニゾロンが使用されることになる。リツキシマブ+ステロイド併用化学療法を行う場合は強い免疫抑制がかかるため治療前には必ずHBs抗原だけではなく、HBc抗体、HBs抗体もチェックし、既往感染ではないかどうかも評価しておく必要がある。化学療法により強い免疫抑制がかかることだけでなく、治療終了後にも免疫が低下した状態が長期間維持されるため、この間にHBVと宿主の免疫との均衡関係がくずれ、いっきにHBVが増殖し、感染肝細胞の広範な壊死が惹起される可能性があるからである。各種化学療法や免疫抑制療法の免疫抑制の程度とHBV抗原・抗体マーカー別の状態に分けた再活性化率を図2に示す。HBs抗原陽性例では核酸アナログ製剤の予防投与をしたうえで治療を開始する。また今回のようにHBs抗原が陰性でもHBc抗体かHBs抗体が陽性なら治療開始前にHBV-DNAを測定し、定量可能なウイルス量であれば核酸アナログの予防投与を行う。もしHBV-DNAが検出感度未満なら、治療開始後から終了後1年間は1か月ごとにHBV-DNAをモニタリングしていき、検出感度以上になった時点で核酸アナログ製剤を開始し、治療終了後も1年間は拡散アナログ製剤の治療を継続することがすすめられている。

図1:HBVキャリアの自然経過
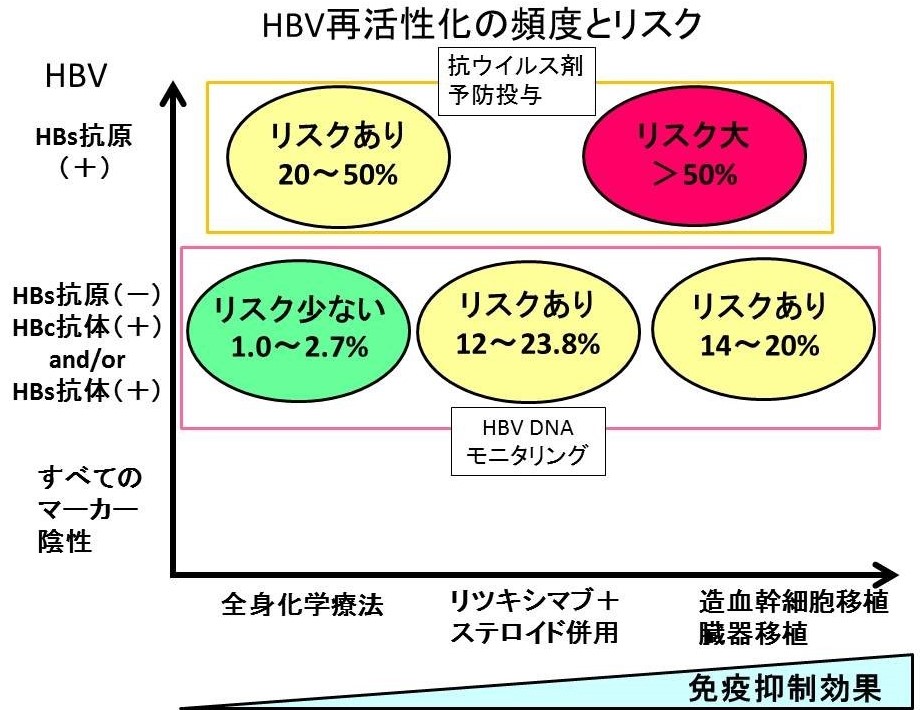
図2:再活性化頻度とリスク
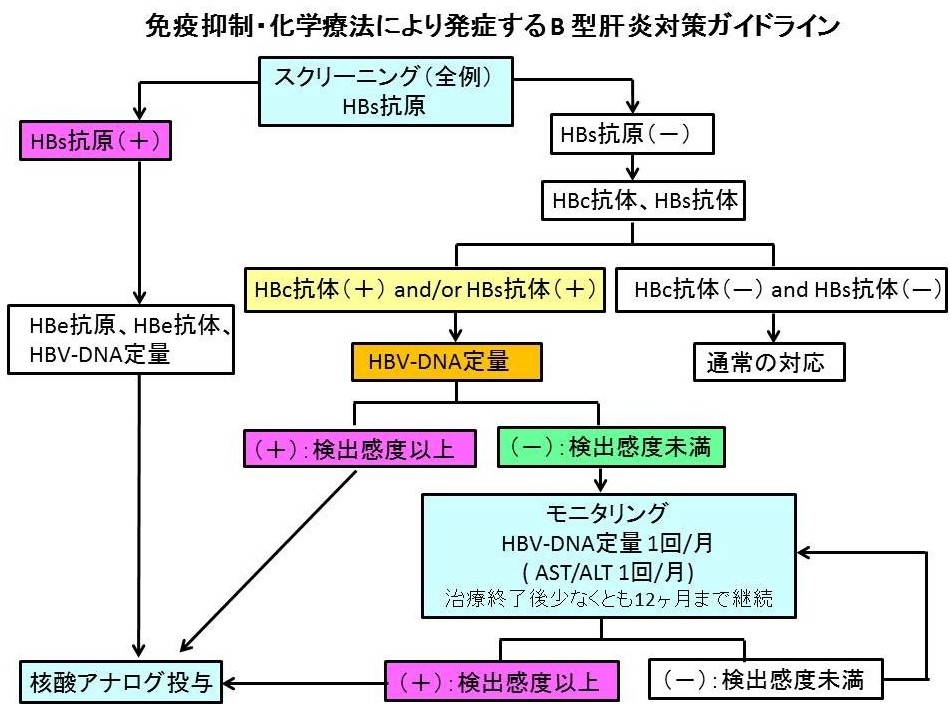
図3:再活性化対策ガイドライン
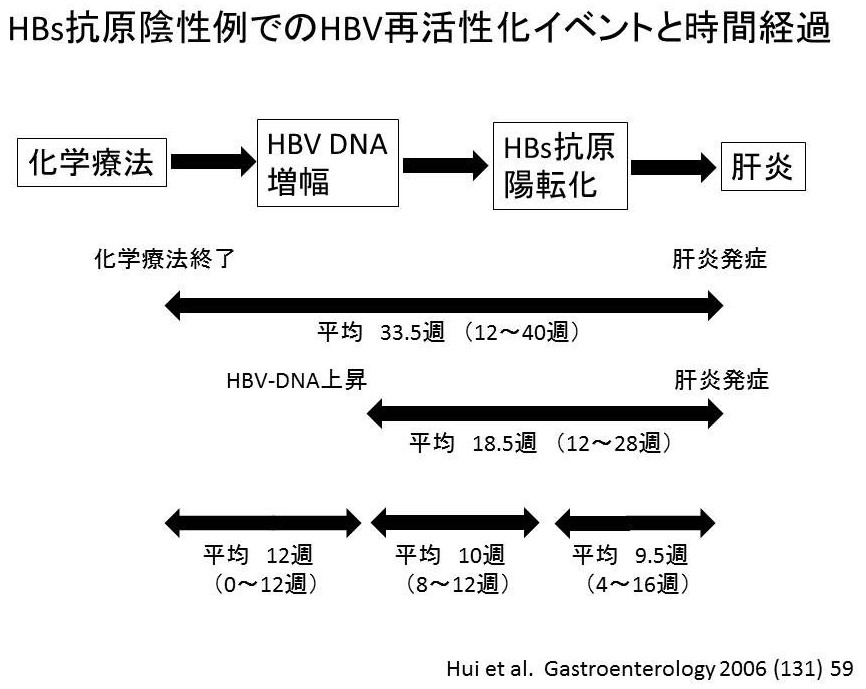
図4:再活性化イベントの経過
解答:(a)(b)
実際の症例では
今回の症例は、化学療法が開始されたのが2009年のB型肝炎ウイルス再活性化に関する診療ガイドラインが出る前の段階で治療が開始されていた症例であったため、実際は問題文に提示された項目しか治療前にチェックされていなかった。ガイドラインが出たあとに血液内科から消化器内科にコンサルトされた症例である。なぜ消化器内科に照会があったか、というと、すでに化学療法を開始されて2年目になっていたのだが、ガイドラインが出てから血液内科でも過去の症例についてひとつひとつHBs抗原をチェックされていたところ、今回の症例では化学療法開始前に陰性であったHBs抗原が、陽性になっていた。おそらくもともとHBVの既往感染者ないしはHBs抗原陰性でHBc抗体高力価陽性の非活動性キャリアであったが、強力な免疫抑制療法の結果、ウイルス量が増加し、HBs抗原が陽転化し、いつ肝炎がおこってもおかしくないところまできていた可能性も十分考えられた(図4)。最後のリツキシマブ+プレドニゾロン併用化学療法が終了して40週目で、幸いにも肝炎は生じていないようであったため、至急HBc抗体、HBs抗体、HBV-DNAをチェックしたところ、HBV-DNAはPCR法で9.0 log copies/mL以上の高ウイルス量であった。ただちに核酸アナログ製剤であるエンテカビル(バラクルード®)の投与を開始し、ことなきを得た。ちなみにこのようなすでに化学療法歴のある患者や免疫抑制剤内服中の患者ではHBc抗体やHBs抗体を測定しても免疫抑制に伴い抗体価が低下しており、偽陰性になる可能性もある。本症例でも消化器内科照会時にはHBc抗体はCLIA法で0.55(正常cut-off index 1.00未満)と陰性であったが、化学療法をすでに行ったあとであったため、偽陰性の可能性が十分考えられた。

