難治性咳嗽で来院
問題112
67歳、女性が難治性咳嗽を主訴に来院された。
【既往歴】喫煙歴:なし。ペット飼育歴:なし。粉塵吸入歴なし。
【現病歴】3~4年前から咳嗽がみられている。胸部レントゲン検査を受けたが特に異常を指摘されていなかった。痰も伴っているが、最初に出る時は黄色で、その後、白色になる。今回胸部レントゲン検査で異常を指摘されて紹介受診となった。
【現症】身長153.0 cm、体重51.6 kg。血圧 140/82 mmHg、脈拍 72/分、整。体温 36.7℃。呼吸数13回/分、SpO2 97%(room air)。皮膚、可視粘膜に貧血なし、黄疸なし。表在リンパ節触知せず。頚静脈怒張を認めない。肺野は両側清、心音は整、病的心雑音聴取せず。下肢に浮腫なし。
【検査所見】血液所見:白血球5600/μL(好中球65.9%、リンパ球27.3%、単球5.0%、好酸球0.7%、好塩基球1.1%)、赤血球465万/μL、Hb 14.3 g/dL、Hct 41.8%、血小板 19.0万/μL。血液生化学所見:CRP 0.02 mg/dL、LDH 278 U/L、AST 23 U/L、ALT 17 U/L、ALP 104 U/L(基準38~113)、γ-GTP 15 U/L、Alb 4.2 g/dL、BUN 13 mg/dL、Cr 0.62 mg/dL、KL-6 5015 U/mL(基準103~500)、SP-D 456 ng/mL(基準<110)。
胸部単純レントゲン写真(図1)、胸部CT(図2)、気管支肺胞洗浄液の外観(図3)を示す。
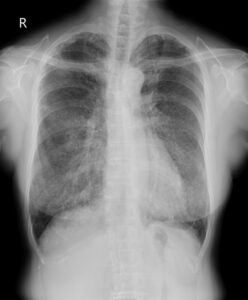
図1
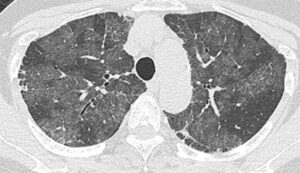
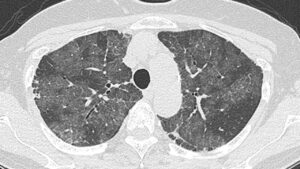
図2

図3
問題
1) 本疾患で機能低下を呈する細胞はどれか。1つ選べ。
(a) Ⅰ型肺胞上皮細胞
(b) Ⅱ型肺胞上皮細胞
(c) 肺胞マクロファージ
(d) 肺胞毛細血管内皮細胞
(e) 気管支平滑筋細胞
2) 本疾患の治療法として正しいのはどれか。1つ選べ。
(a) 抗菌薬
(b) 免疫チェックポイント阻害薬
(c) 肺洗浄
(d) N-アセチルシステイン吸入療法
(e) 副腎皮質ステロイドパルス療法
(類題 2016年総合内科専門医試験)
解説
難治性咳嗽で発症し、胸部レントゲン写真では中~下肺野にかけて淡く透過性が低下した領域を認めている。これを受けて撮影された胸部CTでは両側肺にびまん性で非区域性のすりガラス陰影を認め、その陰影の中の小葉間隔壁の肥厚がみられるためメロンの皮様の陰影、あるいは不揃いの敷石状パターン(crazy-paving pattern)と呼ばれる陰影となっている(図2)。このような陰影を呈する疾患は数多く、現在世界的に流行しているCOVID-19肺炎のようなウイルス性肺炎のほか、ニューモシスチス肺炎、肺胞蛋白症(pulmonary alveolar proteinosis;PAP)、リポイド肺炎、ARDS、急性間質性肺炎、薬剤性肺炎、肺胞出血、細気管支肺胞上皮癌、非特異性間質性肺炎、器質化肺炎、サルコイドーシス、放射線肺炎、過敏性肺臓炎、肺静脈閉塞症、肺水腫、レプトスピラ症、吸引性肺炎、肺胞微石症、菌状息肉症、カポシ肉腫などがあげられる。しかし、このようなCT画像がしっかりあるにもかかわらず、血液検査所見で炎症反応が上がっておらず、臨床像で3年前から持続している咳嗽と喀痰という慢性的な経過で重症感がないこと、血液検査ではKL-6、SP-Dなどの肺線維化マーカーが著増していること、画像的にはやはり特徴的なメロンの皮様の陰影がから考えて、肺胞蛋白症を第1に、肺胞微石症(リン酸Caが肺胞内に蓄積、II 型肺胞上皮細胞にのみあるSLC34A2遺伝子の異常、初期には無症状、非常に稀)、リポイド肺炎(内因性のもので多くは肺癌で閉塞した気管支・リンパ管の閉塞により逸脱した脂質を肺胞マクロファージが貪食し肺胞内に浸潤する病態、外因性ものは油性物質の吸入や誤嚥で生じる)、サルコイドーシス(慢性肉芽腫性病変で慢性的な経過、無症状のものから呼吸困難をきたすものまでさまざま)、非特異性間質性肺炎(50歳未満で咳嗽、呼吸困難で発症、数か月から数年の経過もある)、過敏性肺臓炎(環境因子抗原の感作とその過敏症で生じる、急性、亜急性、慢性がありうる)などを鑑別疾患として考えたい。そこで確定診断としては、気管支鏡を行い、経気管支肺胞洗浄液(bronchoalveolar lavage fluid;BALF)で、米のとぎ汁様あるいはミルク様と表現される白濁した色調を確認し、肺生検では、肺胞腔内にHE染色で好酸性に染まるサーファクタントが充満している像を確認したい。今回の症例では、気管支鏡検査が施行され、BALFが米のとぎ汁様の色調を呈していることが確認された(図3)。残念ながらHE染色やPAS染色は行われていないが、パパニコロウ染色(ヘマトキシリン+オレンジG+エオジンY、ライトグリーンSF、ビスマルクブラウン)ではオレンジGで橙色に、ライトグリーンでは緑色に染まる無構造な滴状物質を多数認め、それらを貪食した泡沫細胞も散見された。悪性細胞は認められず、肉眼所見も含めて肺胞蛋白症として矛盾しない結果と考えた。
肺胞蛋白症(PAP)は肺胞内や終末気管支内などの末梢気腔内にサーファクタント由来物質が異常貯留する疾患の総称である。異常貯留しているサーファクタント由来物質とは、好酸性の顆粒状の蛋白様物質である。本患者のサーファクタントはsurfactant protein A(SP-A)とdipalmitoyl phosphatidylcholine(DPPC)の割合が正常者に比べて多く、これらはいずれも肺胞マクロファージで吸収分解されるものであること、また本患者の肺胞マクロファージの遊走能や貪食能の低下がみられることから、本疾患の病態は、サーファクタントの過剰産生ではなく、分解吸収過程における肺胞マクロファージの機能低下によるものと考えられている。このことは、マクロファージの分化増殖に関わる因子についてのノックアウトマウスを用いた実験でも証明されている。
肺胞蛋白症の病因は、自己免疫性(特発性)PAP、続発性PAP、先天性PAP、未分類PAPの4つに分類される。このうち90%を占める自己免疫性PAPでは、顆粒球マクロファージコロニー刺激因子(GM-CSF)に対する中和抗体(抗GM-CSF抗体)が存在し、これが肺胞マクロファージや好中球の機能低下を起こすと考えられている。従来から原発性あるいは特発性PAPと呼ばれていたもののほとんどで抗GM-CSF抗体が陽性であったことが証明されているが、現在抗GM-CSF抗体は保険未収載であり、もしこの自己抗体が未測定で下記の先天性や続発性PAPが否定されれば従来通り特発性PAP、もし陽性が確認できれば自己免疫性PAPと呼ぶ。今回の症例では疾患特殊性も考慮し、より専門的に本疾患を扱っておられる病院への転院のはこびとなり、主治医の方からは抗GM-CSF抗体もそちらでチェックいただくよう依頼された。続発性PAPは、骨髄異形成症候群やニューモシスチスカリニ肺炎、非結核性抗酸菌症、粉塵吸引、などで続発するが、抗GM-CSF抗体は陰性である。先天性PAPはサーファクタントの分解過程だけでなく生成過程にも何らかの先天的な障害があるのではないかと考えられているが、ほとんどの症例では機序は不明である。抗GM-CSF抗体は陰性である。
初発症状は、労作時呼吸困難、咳嗽、喀痰、体重減少などであるが30%の症例で無症状である。自己免疫性PAPは男女比2:1で発症年齢は男女とも51歳である。検査所見としては、肺線維化マーカーであるKL-6、SP-D、SP-Aが著しく上昇する。一般に炎症反応は上昇しない。胸部CTでは非区域性のすりガラス陰影を認め、その陰影の中の小葉間隔壁の肥厚がみられるためメロンの皮状、あるいはcrazy-paving patternと表現される。自己免疫性PAPの場合、画像所見の割に症状は軽微であることも特徴である。BALFの外観は白濁しており、米のとぎ汁様あるいはミルク様と表現される。肺生検では、肺胞腔内にHE染色で好酸性に染まるサーファクタントが充満し、肺胞マクロファージはサーファクタントを処理できずサーファクタント内に埋もれている。自己免疫性PAP では必ずしも換気障害を呈するわけではなく、重症度に応じて拘束性障害を呈してくる。肺活量の低下に比べ、低酸素血症や拡散能の低下を生じやすい。
治療としては、自己免疫性PAPに対して全肺洗浄あるいは区域洗浄などの洗浄療法が行われている。またGM-CSF吸入療法が試験的に試みられる。自己免疫性PAPの5年生存率は96%、10年生存率は88%であるが、患者はこの間、繰り返し洗浄療法などの治療を要する場合が多い。先天性PAPの予後は極めて悪く、また続発性PAPは自己免疫性PAPに比べて予後は悪い。続発性PAPでは基礎疾患の治療、洗浄療法が行われるが効果は現時点では未確定である。肺移植が実施され移植肺にPAPが再発した報告がある。ステロイドの効果は一般に期待されない。なお選択肢の中でN-アセチルシステイン(NAC)吸入療法は特発性肺線維症(IPF、特発性間質性肺炎)に対して抗線維化目的で行われていたが、最近ではあまり使用されなくなっている。
解答
1)(c) 2)(c)

