半年前から浮腫
問題41
85歳の女性。半月前から下腿浮腫、最近、顔面浮腫も出現し来院。
現症:血圧114/68 mmHg、脈拍 79/分、体温 36.5℃、Spo2 98%。皮膚、可視粘膜に貧血・黄疸なし。頚部リンパ節触知せず。頸静脈怒張なし。呼吸音、心音に異常なし。腹部腸蠕動正常。肝脾触知せず。下腿、顔面に浮腫あり。神経学的に異常を認めず。
検査所見:尿所見:蛋白(2+)、糖(-)、潜血(2+)、尿中蛋白181 mg/dL、6.39 g/g・Cr、尿中β2-マイクログロブリン 17175 μg/L。血液所見:白血球5200/μL、赤血球396万/μL、Hb 11.9 g/dL、Hct 38.7%、血小板17.1万/μL、PT 9.3 sec(117.3%、INR 0.91)、APTT 24.3 sec、血液生化学所見:TP 6.1 g/dL、Alb 2.7 g/dL、IgG 1786 mg/dL(基準870~1700)、IgA 65 mg/dL(基準110~410)、IgM 94 mg/dL(基準33~190)、総ビリルビン0.5 mg/dL、AST 36 U/L、ALT 25 U/L、LDH 243 U/L、BUN 20 mg/dL、Cr 0.72 mg/dL、UA 3.6 mg/dL、空腹時血糖93 mg/dL、Na 140 mEq/L、K 3.9 mEq/L、Cl 104 mEq/L、Ca 8.4 mg/dL、P 2.8 mg/dL、CRP 0.23 mg/dL、血清蛋白分画 Alb 50.2%、α1-glob 4.3%、α2-glob 12.6%、β-glob 7.9%、γ-glob 25.0%。
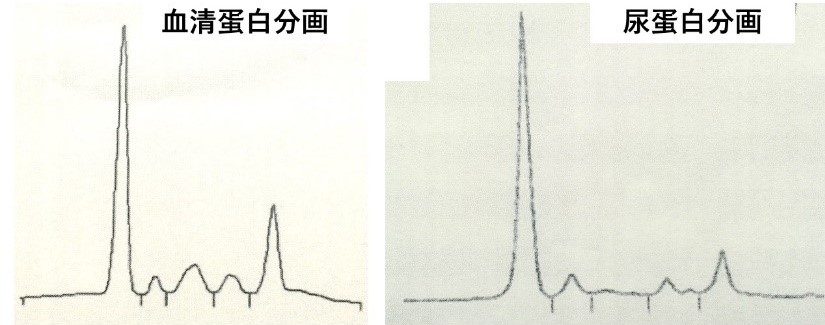
本疾患の予後因子となる血液生化学項目はどれか。1つ選べ。
(a)Ca
(b)IgG
(c)LDH
(d)Hb
(e)CRP
解説(オリジナルは『Dr. Tomの内科症例検討道場』にはないが院内で行った内科症例検討道場で症例301として扱ったもの)
多発性骨髄腫によるネフローゼ症候群の症例である。通常、多発性骨髄腫の場合、高蛋白血症にもかかわらず低アルブミン血症がある、いわゆる蛋白・アルブミン乖離が認められるためγ-グロブリン分画がかなり高いものと推察し、γ-グロブリン分画、IgG、IgA、IgMなどをチェックして多発性骨髄腫という診断がつくことが多いが、今回の場合は、尿中蛋白は181 mg/dL、6.39 g/g・Crとネフローゼ症候群が疑われるようなかなりの蛋白尿があるためか、高蛋白血症は認められない。それでも血清蛋白分画でγ-グロブリン分画上昇が25.0%と上昇しており、γ-グロブリン分画のところにはM-ピークがみられている。これはM蛋白血症があることを意味しており、免疫グロブリンを産生する形質細胞由来の腫瘍である多発性骨髄腫(multiple myeloma; MM)あるいはその前駆病変である単クローン性免疫グロブリン血症(monoclonal gammopathy of undetermined significance; MGUS)が考えられる。これらの病態では単一の免疫グロブリンが腫瘍細胞から大量に産生される。一般に免疫グロブリンは主にγ-グロブリン分画に含まれるため、本疾患患者の血清を通常の電気泳動にかけると、γ-グロブリン分画の上昇がみられるが、単一の免疫グロブリンを大量に産生するため、γ-グロブリン分画内にとがったピークがみられ、これがMピークである(図1)。
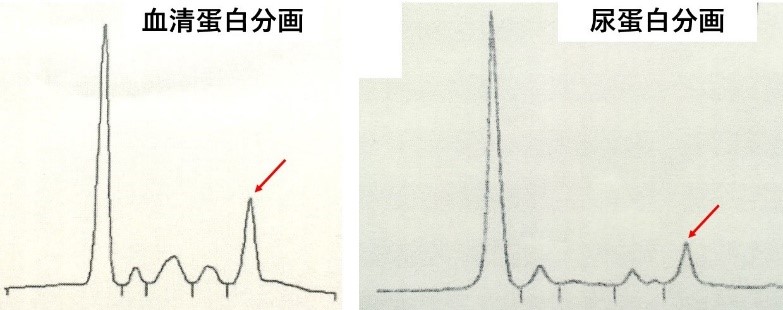
図1:γ-グロブリン分画にMピークがみられ、M蛋白血症があるものと考えられる。
さらに単一の免疫グロブリンということで、次にどの免疫グロブリンかを確認するためγ-グロブリン分画をみる。するとIgG 1786 mg/dlが上昇、さらに今回問題文には提示していないが免疫グロブリンのL鎖のうちλ鎖が 112.00 mg/dlと上昇していたため、IgGλ型M蛋白血症と判明した。確定診断するため、骨髄検査を行った結果、形質細胞の集塊が散見され、核の大小不同などを呈する骨髄腫細胞を11.2%認め多発性発髄腫と診断した(図2)。
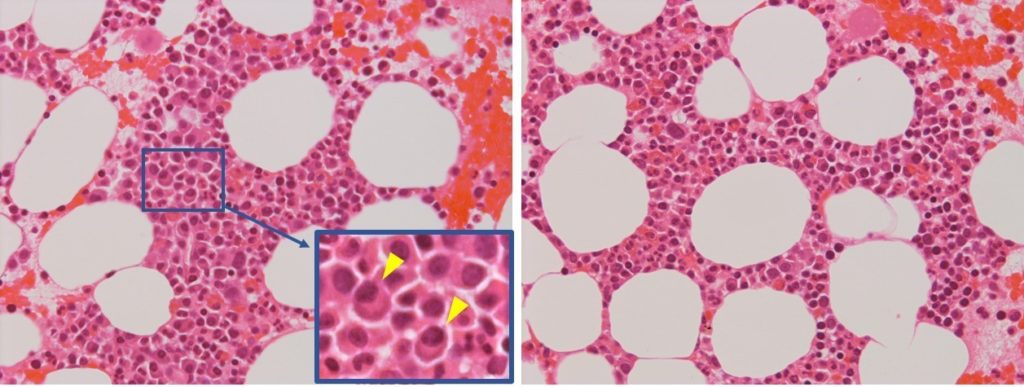
図2:骨髄クロット像(HE染色)。広い細胞質をも持ち核は偏在し、核の周囲が明るく見える(核周囲明庭)形質細胞の特徴を持った骨髄腫細胞が増加している。例えば青枠で囲った範囲には拡大像で示すような細胞がみられている。
多発性骨髄腫の場合、M蛋白となる免疫グロブリンのL鎖(軽鎖)を原料としてアミロイドという異常蛋白が各種臓器に沈着する病態が考えられ、腎障害が生じているのであれば、多発性骨髄腫をベースに生じた腎アミロイドーシスの可能性が考えられた。腎生検が施行された。光顕では糸球体に淡い好酸性の無構造な沈着物を認め、これはダイロン染色(Congo red染色と同様、アミロイドを検出する染色)で橙赤色に染色されたため腎アミロイドーシスと診断された(図3)。
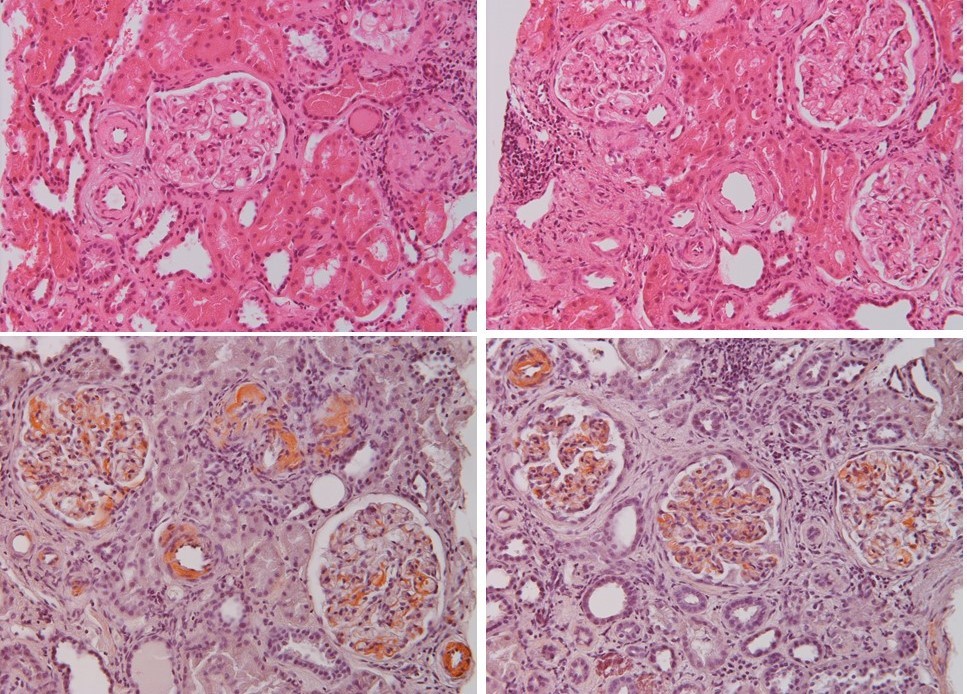
図3:腎生検組織像。上段はHE染色、下段はダイロン染色。糸球体や間質血管壁に淡い好酸性の無構造な沈着物を認め、これはダイロン染色で橙赤色に染色されたため腎アミロイドーシスと診断された。
一般に骨髄造血幹細胞は骨髄中でB細胞に分化してリンパ節に移動し、さまざまな抗原刺激をうけてより成熟したBリンパ球へと成熟するが、一部のB細胞は骨髄に戻り、成熟形質細胞へと分化すると、IgA、G、M、Dなど多種の免疫グロブリンを産生し、血中に放出する。この時、骨髄中で形質細胞となった細胞が腫瘍化すると骨髄腫細胞となり、1種類の異常免疫グロブリン(M蛋白;その種類によって、最も多いIgG型、IgA型、IgD型、IgE型、Bence Jones型に分類され、IgMを産生する細胞は通常は骨髄腫細胞ではなく形質細胞様リンパ球であり、骨病変を伴いにくい点もあって原発性マクログロブリン血症として別疾患として扱われる)を大量に産生する単クローン性の細胞となる。病態としては、骨髄腫細胞から破骨細胞活性化因子(osteoclast activating factor;OAF)が産生されるため骨融解が生じ圧迫骨折、骨打ち抜き像(punched out lesion)などの骨融解、高Ca血症がみられる。また大量のM蛋白が産生されると血液は粘稠度を増して過粘稠度症候群を呈し、またM蛋白は正常の免疫グロブリンのような液性免疫としての活性はないので易感染性となる。さらにこれが各種臓器に沈着することで臓器障害を引き起こす。特に腎アミロイドーシス(アミロイド腎症)はアミロイド蛋白が糸球体に沈着する結果、糸球体障害、ネフローゼ症候群の原因となる。今回の症例はIgGλ型のM蛋白血症がみられているが、これは骨髄腫細胞がIgGを過剰産生している状態であり、これに伴ってL鎖であるλ鎖の産生も過剰に生じている状態と考えられる。一方Bence Jones型の多発性骨髄腫の場合、骨髄腫細胞は完成されたIgGではなく、もっぱら遊離L鎖であるBence Jones蛋白のみを過剰産生しているタイプを指し、逆にIgGの産生は抑制される。Bence Jones蛋白がγグロブリンの構造の中でL鎖のみからなっているため容易に糸球体を通過し、 ①Bence Jones蛋白の尿細管への直接的な障害機序と、②Tamm-Horsfall蛋白との結合によって生じた円柱が尿細管閉塞を起こす機序、により 主に尿細管障害を引き起こす。これを骨髄腫腎という。また骨髄腫では造血障害も生じるが、これは骨髄腫細胞が骨髄内で増殖する結果、正常造血幹細胞が減少し、白血球減少、貧血、時には血小板減少が認められるのである。
多発性骨髄腫に対する治療については、症候性かどうか(下記のCRABうちどれか1つ。[C] 高Ca血症:血清Ca値≧10.5mg/dLまたは基準値以上、[R] Renal failure:血清Cr値>2 mg/dL、[A] Anemia:貧血 Hb<10 g/dLまたは基準値より2 g/dL以下に低下)、[B] Bone lesion:溶骨性病変または骨粗鬆症)を評価し、症候性と判断される場合のみ治療適応となる。今回の症例はもちろんRがあるため症候性である。
予後判定として、もともと血清β2-マイクログロブリンとアルブミン値に基づく国際病期分類が用いられてきたが、これに間期FISH法での高リスク染色体異常(CA)(TP53 del(17)、IgH-FGFR3 t(4; 14)、IgH-MAF t(14; 16)のいずれか)と骨髄腫細胞の増殖能を示唆するLDH値も因子に追加された改訂国際病期分類が用いられている(表1、表2)。
解答:(c)
実際の症例では
●その他の沈着部位の検索として、上部消化管内視鏡検査では肉眼的には異常なかったが、十二指腸粘膜生検ではCongo red染色で一部の血管壁に弱陽性所見がみられ、アミロイド沈着の可能性が示唆された。また心エコーでは求心性対称性左室肥大、右室肥大、房室弁肥厚、心房や心房中隔肥厚など、心アミロイドーシスに特徴的な所見はなかった。

